W termodynamice wyróżnia się trzy stany skupienia materii, są to: stan stały, ciekły i gazowy, który jest również nazywany stanem lotnym. Stan skupienia w jakim występuje dane ciało zależy od czynników zewnętrznych takich jak np. temperatura, czy ciśnienie.
Przykładowo ogrzewanie ciała stałego przy stałej wartości ciśnienia powoduje jego przejście w stan ciekły, a następnie gazowy. Odpowiednie przemiany fazowe noszą w tym przypadku nazwy topnienie i parowanie. Możliwy jest również proces, w którym ciało stałe przechodzi bezpośrednio w stan lotny, nosi on nazwę sublimacji.
W przypadku ochładzania gazu, przechodzi on do stanu ciekłego, a następnie do stanu stałego. Procesy te noszą nazwy skraplanie i krzepnięcie. W przypadku, gdy gaz przechodzi bezpośrednio do stanu stałego z pominięciem fazy ciekłej mówimy o resublimacji.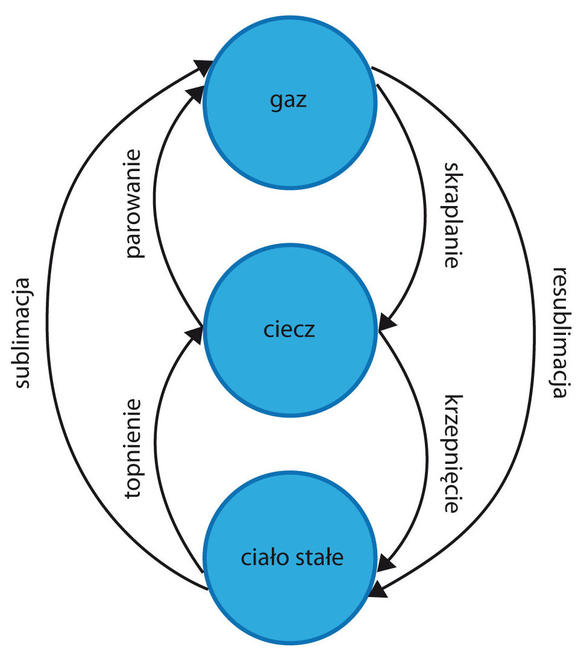
Rys. Monika Pilch
Rys. Zmiany stanu skupienia materii.
Stan skupienia materii zależy od rodzaju wiązań między jej atomami lub cząsteczkami.
W przypadku ciała stałego cząsteczki zajmują ściśle określone położenia (tworzą tzw. sieć krystaliczną), a ich ruch polega na oscylacjach wokół pewnego położenia równowagi.
Dostarczanie do ciała stałego energii (np. w formie ciepła) powoduje wzrost szybkości ruchów termicznych cząsteczek, co skutkuje osłabieniem się wiązań krystalicznych.
W przypadku topnienia wiązania między cząsteczkami są na tyle słabe, że sieć krystaliczna, czyli uporządkowanie cząsteczek, przestaje istnieć i ciało przybiera postać cieczy.
W przypadku parowania ruchy termiczne cząsteczek są już na tyle duże, że powodują zupełne zerwanie wiązań pomiędzy cząsteczkami, więc możliwe jest oddalanie się cząsteczek od siebie na znaczne odległości.
W przypadku gazów odległości pomiędzy cząsteczkami są znacznie większe niż w przypadku cieczy, co powoduje, że gazy można sprężać, natomiast ciecze są bardzo mało ściśliwe.