Aldehydy łatwo ulegają reakcji utleniania, wynika to ze struktury grupy karbonylowej w aldehydach. Wodór połączony z węglem karbonylowym może być łatwo usunięty podczas reakcji utleniania.
Odczynniki utleniające aldehydy:
-odczynnik Jonsa (\(CrO_3\))
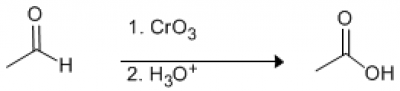
-gorący \(HNO _{3} \) i \(KMnO _{4} \)
- odczynnik Tollensa (\(Ag_2O\))
Odczynnik Tollensa ma szerokie zastosowanie w syntezie, ponieważ pozwala na łagodne utlenienie aldehydu bez naruszania innych grup funkcyjnych w cząsteczce.
Reakcjami wartymi zapamiętania w kontekście związków karbonylowych są próby Tollensa i Trommera, które stosuje się do identyfikacji aldehydów.
2[Ag(NH3)2]+ + HCHO + 3OH- → 2Ag↓ + HCOO- + 2H2O + 4NH3 - próba Tollensa
CH3CH2CHO + 2Cu(OH)2 → CH3CH2COOH + Cu2O↓ + 2H2O - próba Trommera
Aldehydy ulegają również tzw. reakcji Cannizzaro, która jest przykładem dysproporcjonowania (aldehyd ulega jednocześnie utlenieniu i redukcji):

W wyniku utlenienia aldehydu zyskuje się kwas karbonylowy, natomiast redukcja (uwodornienie) prowadzi do powstania alkoholu.
Co więcej, aldehydy ulegają dużej ilości przekształceń wynikających z możliwości addycji nukleofina do karbonylowego atomu węgla (atak pod kątem 45° do płaszczyzny wiązania C=O), wyróżniamy następujące nukleofile: jon hydroksylowy, jon wodorkowy, karboanion, jon alkoksylowy, jon cyjankowy, woda, alkohol, amina, amoniak.
W wyniku wyżej wymienionych reakcji otrzymuje się:
- dla jonu wodorkowego- alkohol drugorzędowy
- dla karboanionu - alkohol drugorzędowy
- dla alkoholi - acetal
- dla aminy - iminy i enaminy
- dla jonu cyjankowego - cyjanohydryny
Charakterystyczną dla aldehydów reakcją jest również kondensacja aldolowa tj. połączeniu się dwóch związków karbonylowych, czego produktem są aldole:

Aldehydy zdolne są również do łączenia się w długie polimery na drodze polikondensacji. Przykładem tworzywa powstałego w ten sposób żywica fenolowo-formaldehydowa.