Znając wzór strukturalny oblicz stężenie % roztworu sacharozy wiedząc, że na 0,5 mola cukru przypada 5L wody
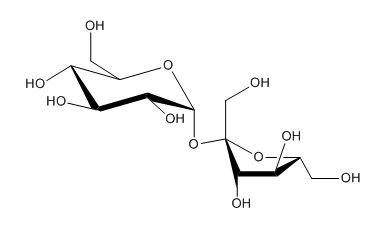
Przygotowano roztwór sacharozy w ten sposób, że na 0,5 mola cukru przypada 5 dm3 wody. Oblicz stężenie procentowe otrzymanego roztworu. Przyjmij, że gęstość wody wynosi 1 g/ml, oraz następujące masy atomowe pierwiastków: MO = 16u, MH = 1u, MC = 12u. Na rysunku poniżej przedstawiono wzór strukturalny sacharozy.
Odpowiedź eSzkola.pl
Michał
Ekspert eSzkola.pl
Obliczenie masy molowej sacharozy:
Msacharoza = 12×12+1×22+16×11 = 342 g/mol
1 mol – 342 g sacharozy
0,5 mola – x g sacharozy
x = 171 g sacharozy
Obliczenie masy wody z gęstości:
5 dm3 = 5000 cm3
mH2O = d×V = 1×5000 = 5000 g
Podstawienie danych do wzoru:
Odpowiedź: Stężenie procentowe otrzymanego roztworu sacharozy wynosi 3,31%.
Dzięki!
3
Znasz odpowiedź na to pytanie?
Wszystkie odpowiedzi (1)
olka
2024-02-26 17:34:05
tak
Dzięki!
1
Odpowiedz
Rozwiąż również:
- Oblicz stężenie molowe roztworu chlorowodoru
- Oblicz liczbę moli hydratu siarczanu(VI) magnezu potrzebną do przygotowania roztworu
- Oblicz ilość mleczanu etakrydyny porzebną do przygotowania roztworu
- Przygotowywanie etanolowego roztworu kwasu salicylowego
- Oblicz masę pięciowodnego siarczanu(VI) miedzi potrzebną do przygotowania roztworu