Miareczkowanie wodorotlenku wapnia
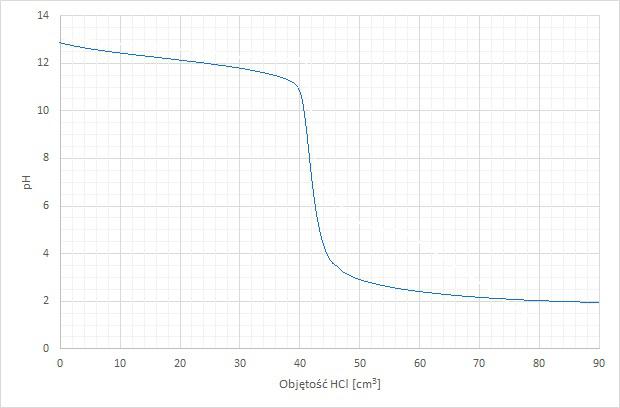
Miareczkowanie jest ilościową metodą analityczną polegającą na kontrolowanym dodawaniu roztworu mianowanego (titranta) do roztworu o nieznanym stężeniu badanej substancji. Titrant reaguje stechiometrycznie z badaną substancją i na tej podstawie wyznacza się ilość zawartej substancji w roztworze. Analizę miareczkową prowadzi się do osiągnięcia punktu równoważności (por. wykres). Oblicz stężenie molowe 150 cm3 roztworu Ca(OH)2 wiedząc, że był miareczkowany roztworem HCl o stężeniu 0,2 mol/dm3, a przebieg reakcji kontrolowano przy pomocy pehametru. Odczytaj niezbędne informacje z wykresu, wyniki podaj z dokładnością do 4. miejsca po przecinku
Odpowiedź eSzkola.pl
Zapisanie równania reakcji:
2HCl + Ca(OH)2 → CaCl2 + 2H2O
Obliczenie ilości moli HCl zużytych w procesie miareczkowania:
n = c × V
n = 0,2 × 0,041 = 0,0082 mola HCl
Obliczenie ilości wodorotlenku wapnia która stechiometrycznie przereagowała z HCl:
2 mole HCl – 1 mol Ca(OH)2
0,0082 mola HCl – x moli Ca(OH)2
x = 0,0041 mola Ca(OH)2
Obliczenie wyjściowego stężenia wodorotlenku wapnia:
c = n/V
c = 0,0041/0,15 = 0,0273 mol/dm3
Odpowiedź: Stężenie wodorotlenku wapnia wynosiło 0,0273 mol/dm3.